Research Fields
1

숙주-미생물 분자상호작용
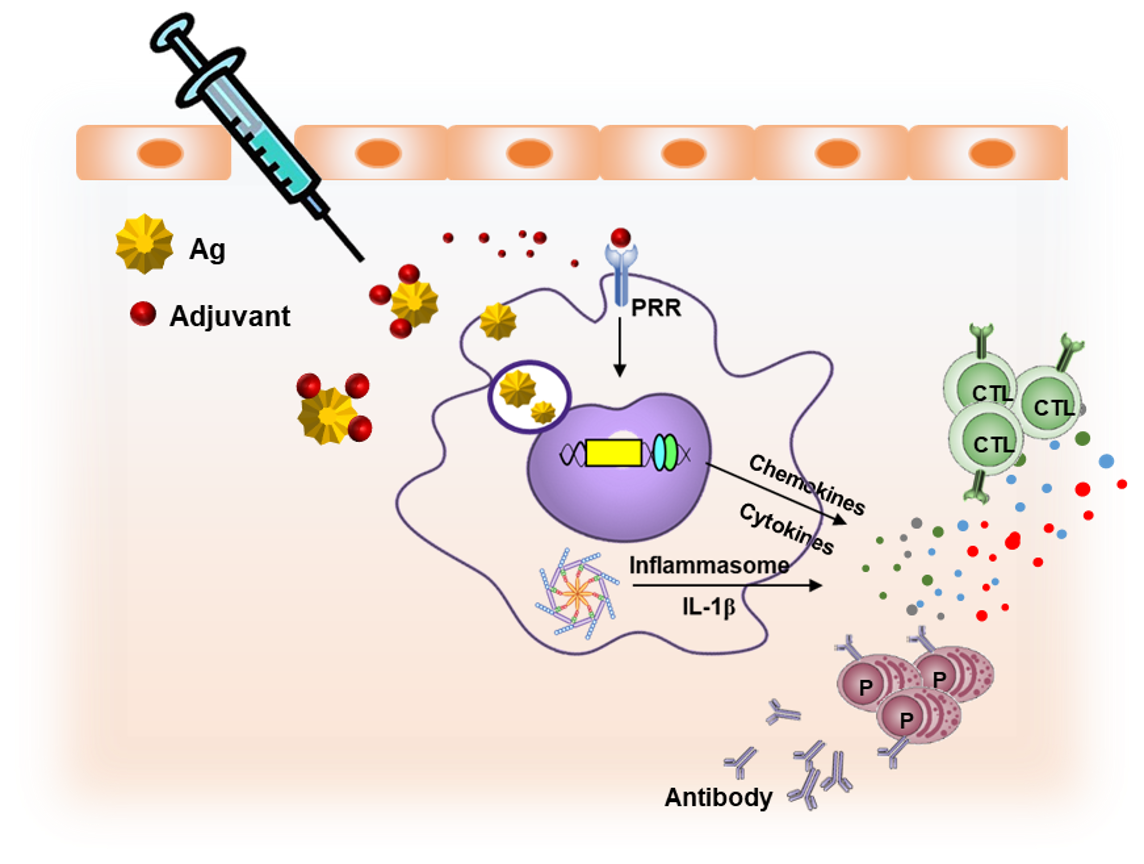
세균에서 MAMP들을 순수 분리하여 분자구조를 밝히고, 다양한 숙주세포에서의 인식과 신호전달 과정을 탐구하여 면역반응 유도과정을 이해하는 연구를 진행하고 있으며, MAMP 결손 돌연변이 균주를 제작하여 동물모델에서 미생물의 감염기전과 숙주 면역반응 유도에서 MAMP의 기능을 연구하고 있다. 이를 통해 감염질환 제어를 위한 표적분자의 발굴과 신개념 감염질환 제어법을 개발하고자 연구를 수행 중이다.
2

미생물의 바이오 필름 제어
세균에 의해 형성된 바이오 필름은 보호막 역할을 하여 항생제나 살균제 및 인체의 면역 시스템으로부터 저항성을 갖게 된다. 본 연구실에서는 병원성 세균의 바이오 필름 형성을 억제 또는 제거할 수 있는 물질을 발굴하고 분자수준에서의 작용 기전을 규명하여 효용성을 높이기 위한 연구를 수행하고 있다. 항생제 내성균의 증가로 항생제 사용의 한계에 부딪치면서, 유산균 유래 물질과 같은 친환경 소재와 박테리오 파지 등 세균과 바이오 필름을 제어할 수 있는 연구를 활발히 진행하고 있다.
3

감염성 골 질환과 MICROBIOTA에 의한 골 대사 조절
세균감염에 의한 염증성 골 질환을 규명하기 위해 세균의 특정 성분과 파골세포(osteoclast) 및 조골세포(osteoblast)와의 관계를 면역학적 관점으로 in vitro, in vivo 실험을 설계하여 연구를 진행하고 있다. 또한 인체 내에 존재하는 미생물총(microbiota)이 골 대사와 어떤 상호작용을 갖는지 연구하고 있으며, 최근에는 뼈 형성 촉진을 유발하는 장내 미생물 유래물질을 규명했다. 위 연구 결과들을 토대로 염증성 골 질환의 병인기전을 정확히 이해하고 질환을 제어할 수 있는 새로운 치료법을 제시할 수 있을 것이다.
4

백신 개발과 효능 평가
수인성 전염병인 콜레라를 예방하기 위한 백신을 모델로, 백신에 의해 유도되는 특이 선천성 면역반응을 규명하였고, 호흡기 감염모델을 적용한 새로운 동물모델을 개발하여 콜레라 백신에 의해 유도되는 획득면역반응에 콜레라 세균과 독소 모두가 중요한 역할을 하고 있음을 규명한 바 있다. 한편, 감염과 암에 대항하는 면역반응 유도에 중요한 역할을 수행하는 수지상세포의 특성과 기능에 대한 심도 있는 기초연구와 함께 면역세포치료제로 개발하기 위한 응용연구도 수행하고 있다.
1
숙주-미생물 분자상호작용
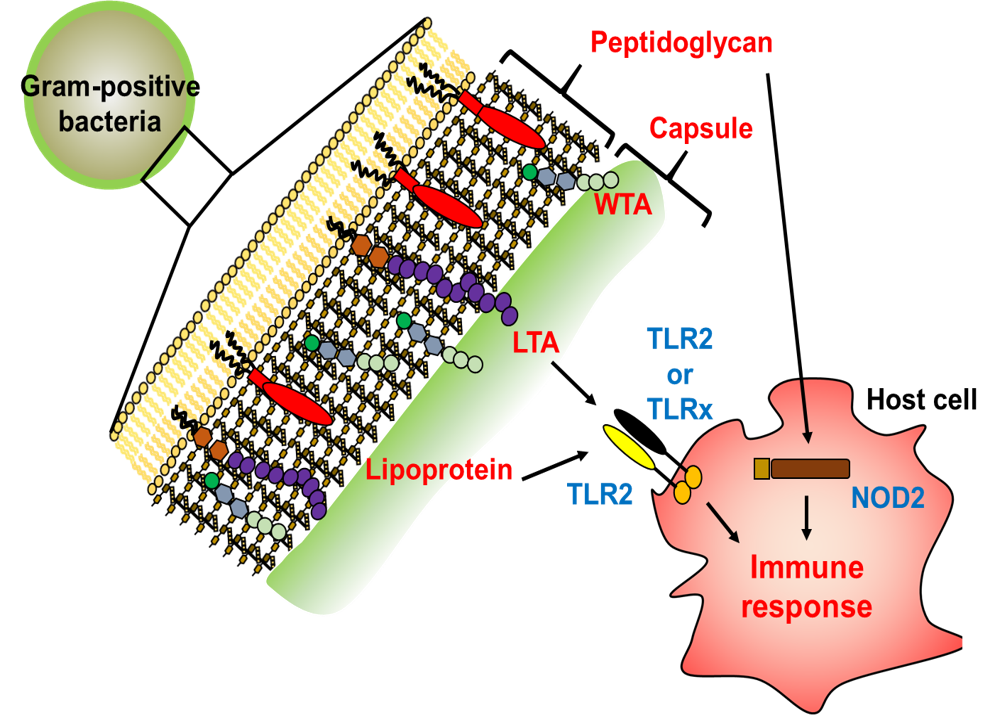
인체와 상호작용을 하고 있는 미생물은 유산균과 같이 인체에 이익을 주는 미생물이 있는가 하면 인체에 치명적인 해를 끼치는 병원성 미생물도 있다. 미생물의 기본 구조가 유사함에도 불구하고 병원성이 다르게 나타나는 이유 중 하나는 lipoteichoic acid, lipopolysaccharide, peptidoglycan과 같은 미생물 특이 분자 패턴(Microbe-Associated Molecular Pattern; MAMP)의 구조에 차이가 있고, 숙주세포는 이것들을 다르게 인식하기 때문이다. 본 연구실에서는, 병원성 세균, 비 병원성 세균, 유익균에서 MAMP들을 순수 분리하여 분자구조를 밝히고, 점막상피세포, 면역세포 등 다양한 숙주세포에서의 인식과 신호전달 과정을 탐구하여 숙주의 면역반응 유도과정을 총괄적으로 이해하는 연구를 진행하고 있다. 아울러, MAMP들이 결손된 돌연변이 균주를 제조하여 실험동물모델에서의 미생물 감염기전과 숙주 면역반응 유도에 있어서 MAMP들의 기능이 무엇인지 연구하고 있다. 숙주–미생물의 분자적 상호작용을 정확히 이해한다면, 감염질환을 효율적으로 제어할 수 있는 표적분자를 발굴할 수 있고, 항생제 오남용으로 인한 부작용을 최소화할 수 있는 신개념의 감염질환 제어법을 개발할 수 있을 것이다.
Microorganisms actively interact with the host through their cell wall structures. Even though commensal and pathogenic bacteria share similar cell wall structures, they induce distinctly different immunological characteristics. Accumulating reports have suggested that microorganisms display unique structures of microbe-associated molecular patterns (MAMPs), thereby augmenting different immune responses by the host. In our laboratory, we prepare highly-pure and structurally-intact MAMPs from various bacteria and investigate their structural differences and their immunological functions in vitro and in vivo. Furthermore, we have generated various MAMP-deficient bacteria to better understand microbes-host interaction. Based on the molecular mechanisms of microbes-host interaction, we can target key molecule(s) to effectively control microbial infections.
2
미생물의 바이오 필름 제어
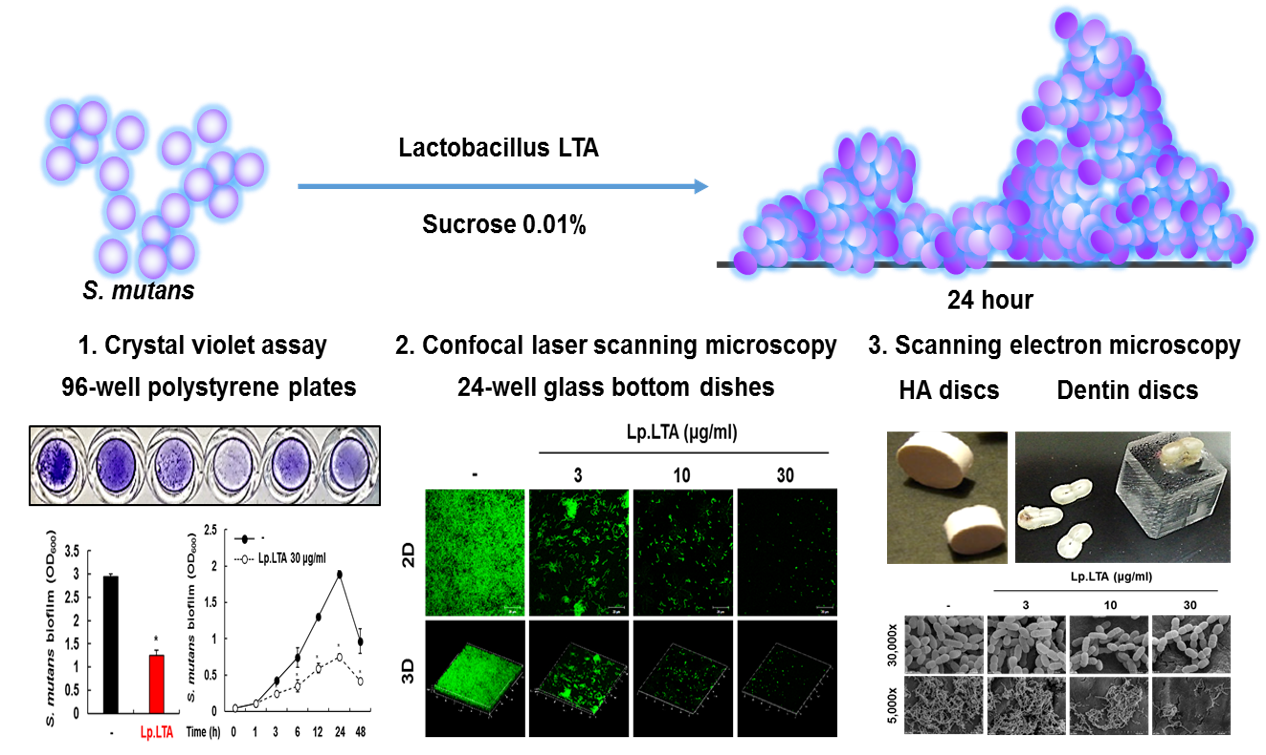
세균은 치아, 보철물, 인공장기와 같은 경조직 뿐만 아니라 소화기와 호흡기 점막과 같은 연조직 표면에 부착하여 고착 상태의 군집인 바이오 필름을 형성할 수 있다. 세균이 만들어내는 다당체 기질에 세균들이 달라붙어 단단하게 형성된 바이오 필름은 보호막 역할을 하여 항생제나 살균제 및 인체의 면역시스템으로부터 저항성을 지니게 된다. 바이오 필름은 외부 환경으로부터 세균을 보호하고 증식을 유지시킬 뿐만 아니라 바이오 필름 내 미생물간의 상호 커뮤니케이션을 통해 독소 생산과 항생제 내성 유전자의 교환을 매개하는 역할을 한다고도 알려져 있다. 본 연구실에서는 병원성 세균의 바이오 필름 형성을 억제 또는 제거할 수 있는 물질을 발굴하고 분자수준에서의 작용 기전을 규명하여 효용성을 높이기 위한 연구를 수행하고 있다. 특히, 항생제 내성균의 증가로 항생제 사용의 한계에 부딪치면서, 유산균 유래 물질과 같은 친환경 소재로 바이오 필름을 제어할 수 있는 연구를 활발히 진행하고 있다. 바이오 필름 제어 연구는 항생제를 대체할 새로운 패러다임의 연구로서, 의료용 소독제, 감염 예방제, 동물용 항균제, 사료 첨가제, 식품위생소재 등 다양한 분야에 활용될 수 있을 것이다.
Bacteria can bind not only to hard tissues such as teeth, implant, or an artificial organ but also to soft tissues such as mucous membrane and organs to develop biofilm formation. Bacterial biofilm is a form of bacterial aggregate which confers protection against antibiotics, detergent and host immune defense. Our study focuses on the identification of biological substances to restrict and/or eliminate bacterial biofilm formation and elucidate the action mechanisms at the molecular level. Since the overuse or misuse of antibiotics generate antibiotic resistant bacteria, alternative strategy to replace conventional antibiotics is in demand. Our laboratory has found biological substances from a beneficial bacterium, Lactobacillus, which effectively inhibited the formation of pathogenic bacterial biofilm, and we are extensively studying the molecular mechanisms of action for the inhibitory effect on the biofilm formation. The Lactobacillus-derived substances have promising uses in the field of medicine, feed additives and food hygiene materials to prevent the formation of bacterial biofilm.
3
감염성 골 질환 병인기전과 골 대사 조절
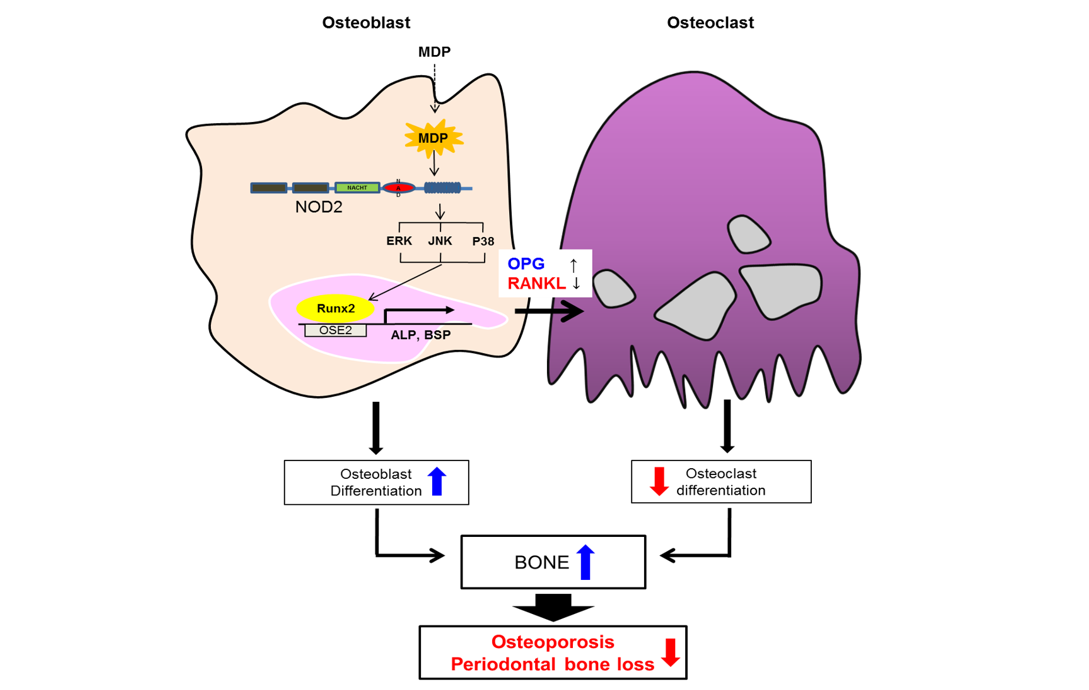
골 조직에서는 파골세포가 불필요한 뼈를 파괴/흡수시키고 조골세포가 새로운 뼈를 만들어내는 재형성 과정(bone remodeling)을 끊임없이 반복하며 항상성을 유지하고 있다. 파골세포와 조골세포의 분화와 활성이 균형과 조화를 이루지 못하고 항상성이 깨질 경우 골다공증(osteoporosis)이나 골석화증(osteopetrosis)이 유발될 수 있다. 뼈 속에는 골 세포 외에도 조혈모세포와 다양한 분화단계에 있는 면역세포들이 공존하며 서로 밀접하게 상호작용을 하고 있다. 본 연구실에서는, 세균감염에 의한 염증성 골 질환이 어떠한 과정에 의해 유발되는지, 세균의 어떤 구성물질이 골 질환 유발에 중요한지를 다양한 in vitro 및 in vivo 실험모델을 활용하여 연구하고 있다. 최근에는, 세균의 지질단백질이 염증성 골 질환을 유발하는 중요한 구성성분임을 규명한 바 있다. 한편, 인체 내에 존재하는 미생물총(microbiota)이 골 대사에 어떠한 영향을 주는지 연구하고 있으며, 장내 미생물에서 유리된 물질이 뼈 형성을 촉진할 수 있다는 연구결과를 확보하여 작용기전 연구와 함께 골 질환 예방 및 치료제로서의 응용 연구를 수행하고 있다. 이러한 연구는 치아 우식, 치주질환, 류마티스성 관절염과 같은 염증성 골 질환의 병인기전 이해와 골 질환 예방 및 치료제 개발을 위한 핵심 타겟 발굴에 기여할 것이다.
Bone tissues maintain homeostasis through continuous bone remodeling, a process in which osteoclasts break or absorb mature bone tissues while osteoblasts form new bone tissues. The bone consists of not only osteoblasts but also hematopoietic stem cells and various immune cells at various division stages which closely interact with each other. Using in vitro and in vivo models, our laboratory broadly studies inflammatory bone diseases caused by unbalanced bone remodeling and identifies the bacterial components responsible for the inflammatory bone diseases. Moreover, we explore the effect of intestinal microbiota on bone metabolism, especially, a specific bacterial component or microbial metabolite contributing to bone formation which may prevent several bone diseases such as osteoporosis, rheumatoid arthritis, dental carries and periodontal diseases.
4
백신 개발과 효능 평가
감염질환을 효과적으로 예방할 수 있는 백신을 개발하기 위해서는 백신에 의한 면역반응 유도과정을 이해해야 하고, 인체에서 백신의 효능을 정확히 측정할 수 있는 신뢰성 있는 측정방법을 확보하여야 한다. 본 연구실에서는 수인성 전염병인 콜레라를 예방하기 위한 백신을 모델로, 백신에 의해 유도되는 특이 선천성 면역반응을 규명하였고, 호흡기 감염모델을 적용한 새로운 동물모델을 개발하여 콜레라 백신에 의해 유도되는 획득면역반응에 콜레라 세균과 독소 모두가 중요한 역할을 하고 있음을 규명한 바 있다. 또한, 인체 혈액에서 콜레라 백신의 효능을 효율적으로 측정할 수 있는 측정법을 개발하였고, 인도와 베트남에서 실시된 콜레라 백신의 임상시험에 참여하여 면역학적 효능 평가를 담당함으로써 세계보건기구의 사용승인을 획득하는 데에 일조하였다. 또한, 비강을 통해 접종한 탄저백신에 의해 점막면역과 전신면역반응이 동시에 유도되며, 면역기억반응 유도를 통해 장기간 면역력이 지속됨을 보고한 바 있다. 최근에는, 방사선을 조사하여 제조한 폐구균백신이 포름알데히드와 열처리를 통해 제조한 사균백신보다 면역 효능이 우수함을 알아내어, 92가지 혈청형에 모두 작용할 수 있는 범용백신개발을 위한 연구를 수행하고 있다. 한편, 감염과 암에 대항하는 면역반응 유도에 중요한 역할을 수행하는 수지상세포의 특성과 기능에 대한 심도 있는 기초연구와 함께 면역세포치료제로 개발하기 위한 응용연구도 수행하고 있다.
In order to develop vaccines that can effectively prevent infectious diseases, it is necessary to understand the immunogenic mechanisms and to identify reliable methods to accurately measure the efficacy of vaccines. Recently, our laboratory has established an advanced animal model for studying the efficacy of cholera vaccine and explore the enhanced immunogenicity of cholera vaccine based on the interaction of cholera vaccine and intestinal metabolites. We also developed a highly-advanced method to measure the efficacy of cholera vaccine and contributed to the development of effective cholera vaccine approved by World Health Organization. In addition to cholera vaccine, we established vaccination for the enhancement of long-term effect of anthrax vaccine. Recently, our laboratory focuses on the development of advanced pneumococcal vaccines such as irradiated vaccines which is different from traditional manufacturing process by studying the association of innate immunity with acquired immunity. On the other hand, we are also interested in dendritic cells because they play a pivotal role in the modulation of immune responses by linking innate and adaptive immune responses. We study phenotypes and immuno-modulatory functions of dendritic cells that are generated in various conditions for identifying and preparing medically-useful dendritic cells to be used as a cell-based therapy.